
全部
▼
搜索
熱搜:
位置:中冶有色 >
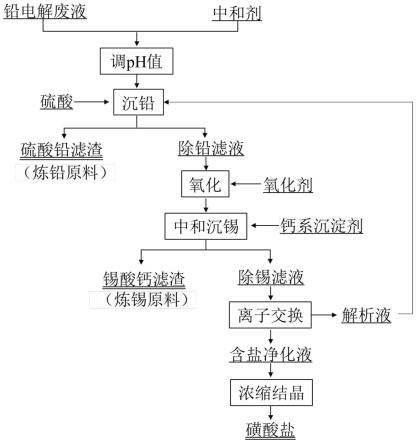
> 甲基磺酸體系鉛電解精煉廢液凈化方法
 600
編輯:中冶有色技術(shù)網(wǎng)
來源:中南大學(xué)
600
編輯:中冶有色技術(shù)網(wǎng)
來源:中南大學(xué)
 分享 0
分享 0
 舉報(bào) 0
舉報(bào) 0
 收藏 0
收藏 0
 反對 0
反對 0
 點(diǎn)贊 0
點(diǎn)贊 0

 中冶有色技術(shù)平臺
中冶有色技術(shù)平臺 2025年03月28日 ~ 30日
2025年03月28日 ~ 30日  2025年03月28日 ~ 30日
2025年03月28日 ~ 30日  2025年03月29日 ~ 31日
2025年03月29日 ~ 31日  2025年04月11日 ~ 13日
2025年04月11日 ~ 13日  2025年04月27日 ~ 29日
2025年04月27日 ~ 29日 
